Li7La3Zr2O12 고체전해질의 이종 도핑 효과에 따른 구조적, 전기적 특성 연구
Investigating the Effect of Co-doping on Structural and Electrical Properties of Li7La3Zr2O12 Solid Electrolyte
Article information
Trans Abstract
Garnet-type Li7La3Zr2O12 (LLZO) has garnered significant attention for solid-state Li-ion batteries due to its commendable Li-ion conductivity, wide electrochemical window, and exceptional chemical and thermal stability. Nonetheless, challenges related to structural instability and air stability persist, impeding its market expansion. Herein, we explore the effects of co-doping (Ga with Sc/Y/In/Er) on the crystal structure and Li-ion conductivity of LLZO through x-ray diffraction (XRD), scanning electron microscope (SEM), and AC impedance measurements. XRD refinement confirms the formation of pure-phase samples with a cubic crystal structure. SEM analysis reveals a dense microstructure with grain sizes exceeding 200 μm and a relative density approaching∼94%. While Ga/Sc and Ga/Y doped LLZO exhibit relatively lower Li-ion conductivity, Ga/Er and Ga/In doped samples demonstrate high conductivity more than 1 mS/cm at room temperature (25°C). Thus, the judicious selection of dopants emerges as an effective strategy for enhancing conductivity in all-solid-state batteries.
1. 서론
리튬 이온 배터리는 높은 에너지 밀도, 장수명, 빠른 충전으로 경쟁력 있는 에너지 저장 솔루션이다.[1,2] 그러나, 가연성 액체전해질에 의해 발생하는 열적 폭발과 관련된 안전 문제들이 전기자동차와 같은 수송용 분야에서의 응용 확대를 저해해왔다. 이러한 문제를 해결하기 위해, 액상전해질 대신 무기 고체전해질을 이용하는 전고체전지에 관한 연구가 활발히 일어나고 있다.[3,4] 다양한 유형의 무기 고체전해질 중에서, 가넷형 Li7 La3 Zr2 O12 (LLZO)는 뛰어난 특성으로 주목받고 있다. 이러한 특성으로는 높은 이온전도성(∼1 mS/cm),[5,6] 리튬 금속 전극과의 우수한 화학적 안정성,[7] 넓은 전기화학적 창(∼5V),[8] 낮은 전자전도성[6,9]이 있다. LLZO는 두 가지 결정 구조, 즉 입방체(공간 군:
또한, 가넷 고체전해질의 성능을 더욱 향상시키기 위해 이종 도핑(co-doping) 전략이 연구되었다.[9,29,30] 예를 들어, Zr 위치에 Nb와 Y[31], 또는 Ga와 Sr[32]가 이온전도성을 증가시키고 공기 중 안정성을 향상시킬 수 있다는 것이 보고되었다. Gai 등은 Zr-위치에 Nb와 Y를 동시에 치환한 것이 공기 중에서 높은 안정성을 가지는 입방체 구조를 보인다고 보고하였다.[31] 그들은 Li7 La3 ZrNb0.5 Y0.5 O12의 전도성 (∼0.7 mS/cm)이 공기 노출 후 1.5 개월 동안 유지되는 것을 발견하였다. Kobi 등은 Al/Mg 이종 도핑된 LLZO가 Li/LLZO 인터페이스의 계면저항을 줄이는 데 효과적임을 밝혀내었다.[30] Shen 등은 Ga와 Sr의 이종 도핑으로 LLZO에서 높은 이온전도성∼0.55 mS/cm이 발현됨을 발견하였다.[32] Ga 도핑은 실온에서 안정적인 입방체 상의 형성과 3D Li 이온 전송 채널의 구축을 유도한다. 반면, Sr 도핑은 구조의 미세변화와 Li 이온 농도의 증가를 일으킨다. 마찬가지로, Xu 등[33]은 Ta/Ce 이종 도핑된 Li6.4 La3 Zr1.4-x Ta0.6 Ce x O12가∼1.05 mS/cm의 높은 Li 이온 전도성을 나타낸다는 것을 밝혀내었다. 더불어 리튬 이동채널의 최적화에 의해 리튬 금속 전극에 대한 우수한 안정성도 보고하였다.
위의 연구결과를 정리하면, 이종 도핑이 결정구조를 안정화시킬 뿐만 아니라 LLZO의 Li 이온 전도성과 공기 중 안정성을 향상시키는 것을 알 수 있다. 따라서, 다양한 도펀트의 조합으로 구조를 안정화시키고 이온 전도성을 증대시킬 수 있을 것으로 사료된다. 본 연구에서 LLZO의 Li 자리에 Ga 도핑과 Zr 자리에 Sc, Y, In, 또는 Er을 이종 도핑하는 새로운 이종 원소 도핑 전략을 사용하였다. 분말 (Li6.25 Ga0.25 La3 Zr1.95 M0.5 O12 (M = Sc, Y, In, Er)) 합성은 통상적인 고상 반응 법을 이용하여 진행하였으며, XRD, SEM의 기초분석을 진행하였다. 전도도는 교류 임피던스법을 이용하여 분석하였다.
2. 실험방법
Li6.25 Ga0.25 La3 Zr1.95 M0.5 O12 (M = Sc, Y, In, Er) 화합물은 Li2 CO3 (Soekawa Chemicals, 99.9 %), La2 O3 (High Purity Chemicals, 99.9 %), ZrO2 (Samchun Chemicals, 99.9 %), Sc2 O3 (Alfa Aesar, 99.9 %), Y2 O3 (High Purity Chemicals, 99.9 %), In2 O3 (Alfa Aesar, 99.9 %), Er2 O3 (Sigma Aldrich, 99.9 %)을 포함하는 고순도 화학물질의 화학량론적 혼합을 사용하여 고상합성법을 통해 합성했다. 하소 및 소결 중의 리튬 손실을 보상하기 위해 Li2 CO3 (10 wt%)를 첨가했다. 혼합물은 이소프로판올에 지르코니아 볼을 넣어 볼 밀링한 후, 공기 중에서 950° C에서 6시간 동안 하소했다. 그 후, 하소된 분말은 입자 크기를 줄이기 위해 추가로 볼 밀링을 진행했다. 직경이 8 mm, 두께가 2 mm의 치밀한 펠릿은 1200° C에서 냉간 등방압 가압법 분말을 소결하여 제작했다. 측정에 앞서 다양한 입자 크기의 SiC 연마재를 사용하여 펠릿을 원하는 두께로 연마했다. 펠릿의 미세 구조는 전계방출형 주사 전자현미경(FE-SEM, ZEISS Sigma 500)을 사용하여 관찰하였다. 시료의 상은 10–60 °의 2θ 범위에서 Cu-Kα 광원을 장착한 Rigaku X-선 회절분석기 (X-ray diffraction, XRD)를 사용하여 평가했다. 시료의 결정 구조는 FullProf 소프트웨어를 사용하여 분석했다. 리튬이온 전도성은 약 10–65° C의 온도 범위와 1 Hz에서 5 MHz의 주파수 범위에서 300 mV AC 신호를 적용하여 Zurich Instruments의 MFIA 분석기를 사용한 전기화학 임피던스 분광법 (EIS)을 사용하여 측정했다.
3. 결과 및 논의
시료의 전기적 특성은 기공도, 입자 크기, 입계 및 펠릿의 상대 밀도에 크게 의존한다.[6,24] 따라서, 좋은 미세구조를 얻기 위해서는 합성 및 소결 변수를 최적화하는 것이 중요하다. 직경이 8 mm이고 두께가 2 mm인 소결 전 펠릿은 200 MPa에서 냉간 등방압으로 압축되었으며, 이후 1200° C에서 소결되었다. Ga3+/Sc3+, Ga3+/Y3+, Ga3+/In3+, 및 Ga3+/Er3+ 가 이종 도핑된 LLZO 펠릿의 소결 거동, 치밀화 과정, 및 미세 구조의 변화를 분석하기 위하여 FE-SEM를 이용하였다. 이종 도핑된 전해질의 단면 이미지를 Fig. 1에 나타내었다.

SEM images for a. Ga3+/Sc3+, b. Ga3+/Y3+, c. Ga3+/In3+, and d. Ga3+/Er3+ codoped LLZO, revealing dense microstructure
SEM 이미지를 통해 모든 시료에서 200 μ m이상의 큰 결정립이 형성되었음을 알 수 있다. 또한, 고온 소결 시 리튬 증발로 인해 결정립 내부에서 3차원적 공공이 관찰된다. 상대 밀도는 94% 이상으로 고밀도 펠릿으로 형성되었다. 결정립계에서 불순물 상의 편석(segregation)은 관찰되지 않았다.
Fig. 2는 1200° C에서 소결된 Ga3+/Sc3+, Ga3+/Y3+, Ga3+/In3+, Ga3+/Er3+ 이종 도핑된 LLZO 시료의 XRD 패턴을 보여준다. 모든 시료의 회절 피크 분석을 통해 목적 상인 입방체 가넷 상 (PDF#45-0109)이 형성되었음을 알 수 있었다. La2 Zr2 O7, Li2 CO3, Li2 ZrO3의 불순물 상과 Ga, Y, In, 또는 Er의 산화물은 관찰되지 않았다. 이는 LLZO에 도펀트가 성공적으로 치환되었음을 나타낸다. Ga3+를 Sc3+, Y3+, In3+, 또는 Er3+로 도핑할 때의 결정구조 변화를 이해하기 위해 XRD 데이터의 리트벨트 분석을 수행하였다. 구조적 피팅은 LLZO에 대해 Wagner 등[34]에 의해 보고된
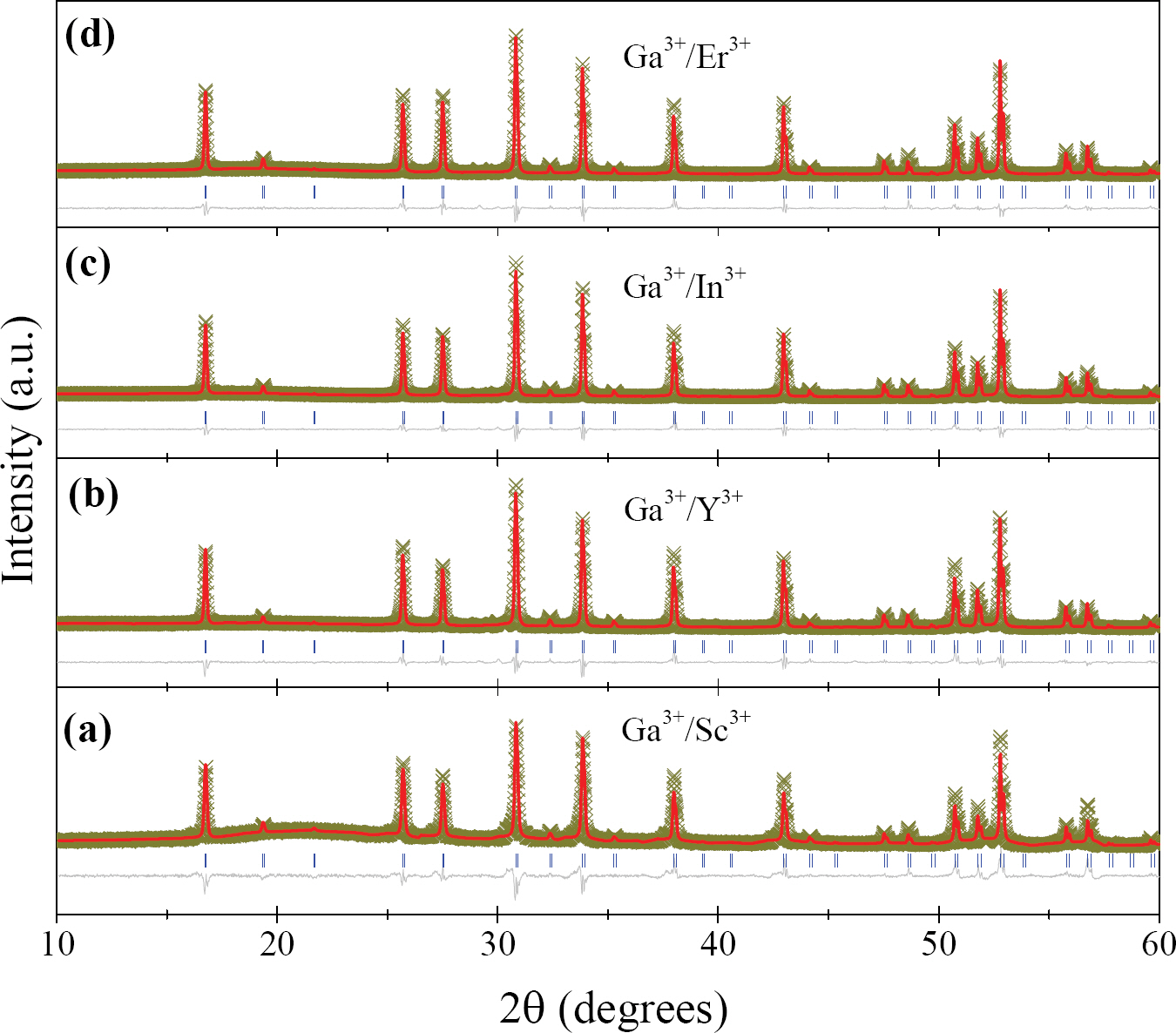
XRD patterns along with Rietveld refinement fits for a. Ga3+/Sc3+, b. Ga3+/Y3+, c. Ga3+/In3+, and d. Ga3+/Er3+ codoped LLZO

Unit cell dimension, selected bond lengths, and R-factors for Ga3+/Sc3+, Ga3+/Y3+, Ga3+/In3+, Ga3+/Er3+ codoped LLZO obtained from Rietveld analysis
Ga3+/Sc3+, Ga3+/Y3+, Ga3+/In3+, 및 Ga3+/Er3+가 이종 도핑된 LLZO 시료의 이온 전도도를 평가하기 위해 교류 (AC) 임피던스를 측정하였다. 25° C에서 측정된 나이퀴스트 플롯을 Fig. 3. a에 나타내었다. 이종 도핑된 모든 시료의 그래프는 고주파 영역에서 하나의 반원을 나타나고 저주파 영역에서 뚜렷한 직선 형태를 보여준다. 저주파 영역에서 실수축 (x-축)에 대한 절편은 시료의 전체 저항이다. Fig. 3. a에서 나타난 바와 같이, Ga3+/Sc3+가 이종 도핑된 LLZO에서 높은 저항 값이 측정되었으며, 반면에 Ga3+/In3+, 및 Ga3+/Er3+가 이종 도핑된 LLZO 시료는 상대적으로 낮은 저항 값이 측정되었다. 리튬 이온 전도도 (σ)은 전체 저항 (R)으로부터 계산하였다.
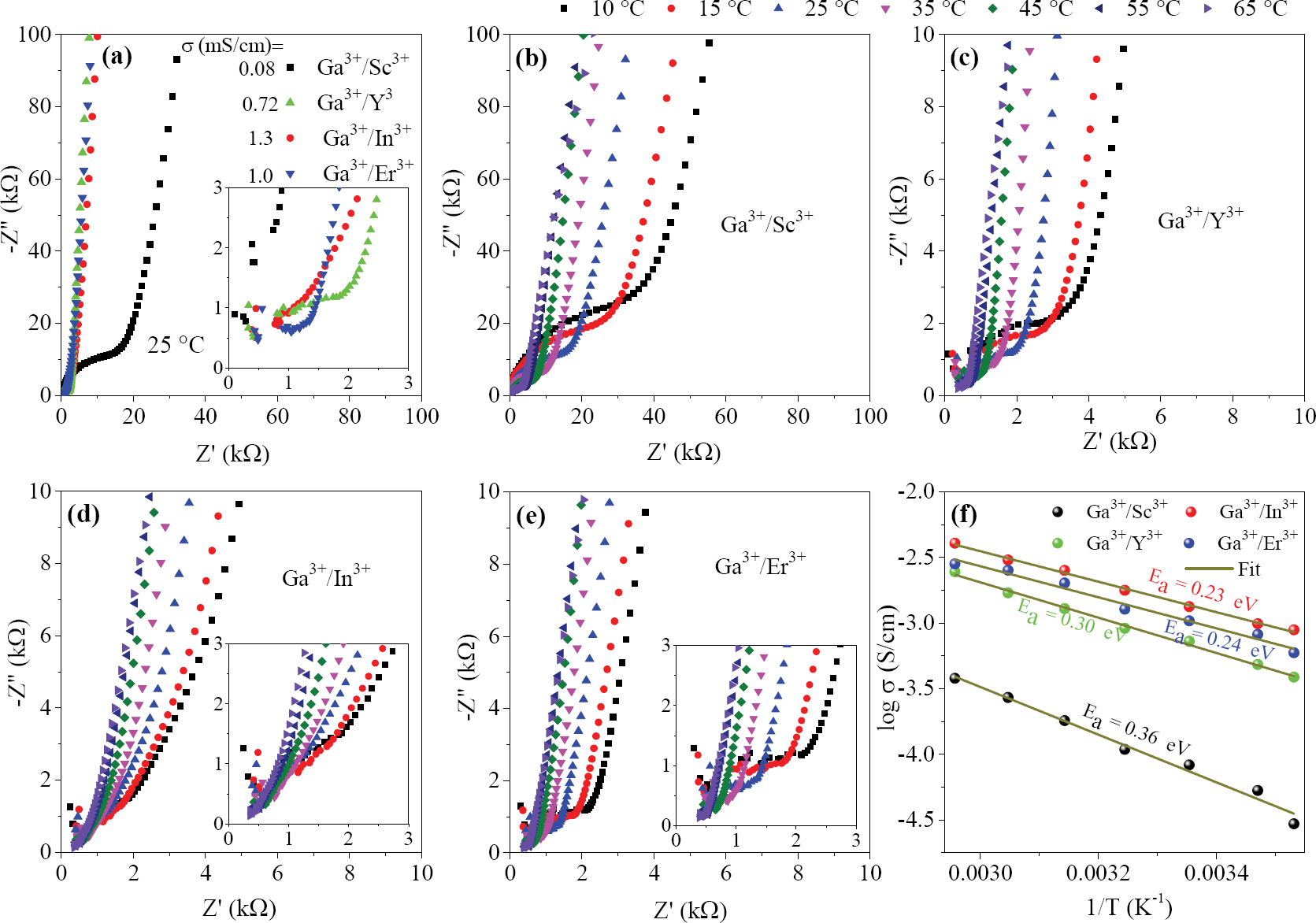
Electrical properties of Ga3+/Sc3+, Ga3+/Y3+, Ga3+/In3+, and Ga3+/Er3+ codoped LLZO: a. Nyquist plots measured at 25 C. Temperature-dependent Nyquist plots of b. Ga3+/Sc3+, c. Ga3+/Y3+, d. Ga3+/In3+, e. Ga3+/Er3+ codoped LLZO in the temperature range 10-65℃, and f. the corresponding Arrhenius plots. The inset represents the magnified view of impedance spectra in the high-frequency region.
리튬 이온 이동의 장벽을 더 이해하기 위해, 모든 시료에 대하여 다양한 온도에서 AC 임피던스를 측정하였다: 10, 15, 25, 35, 45, 55, 65° C(Fig. 3. b-d). 이에 따라 이온 전도도를 계산하였으며, 온도에 따른 이온 전도도는 Fig. 3. f에 나타내었다. 관심 온도 범위에서 ln σ vs. 1/T 그래프에서 선형 관계를 확인하였다. 그리고 이 데이터를 하기 Arrhenius 식에 따라 피팅하였다.
4. 결론
본 실험에서 Ga3+/ Sc3+, Ga3+/Y3+, Ga3+/In3+, 및 Ga3+/Er3+ 이종 도핑에 대한 Li6.25 Ga0.25 La3 Zr1.95 M0.5 O12 (M = Sc, Y, In, Er)의 이온전도도 특성 변화를 연구하였다. XRD 패턴의 리트벨트 분석을 통해 결정 구조를 분석하였으며, 모든 시료에 대해
CONFLICTS OF INTEREST
There are no conflicts to declare.
ACKNOWLEDGEMENTS
이 성과는 정부(과학기술정보통신부)의 재원으로 한국연구재단의 지원을 받아 수행된 연구임(No. RS-2023-00236572). 본 연구성과물은 2024년도 정부(교육부)의 재원으로 한국연구재단의 지원을 받아 수행된 기초연구사업임(No. RS-2023-00249335).
References
Biography

⊙⊙ 모하마드 나시르
⊙ 2009년 Aligarh Muslim 대학교 물리학과 학사
⊙ 2011년 Aligarh Muslim 대학교 물리학과 석사
⊙ 2013년 Aligarh Muslim 대학교 나노기술학과 석사
⊙ 2019년 인도공과대학교 물리학과 박사
⊙ 현재 단국대학교 박사 후 연구원

⊙⊙ 서 준
⊙ 2019년 대전대학교 신소재공학과 학사
⊙ 2021년 단국대학교 신소재공학과 석사
⊙ 현재 단국대학교 신소재공학과 박사과정 재학

⊙⊙ 박 준 서
⊙ 2023년 단국대학교 신소재공학과 학사
⊙ 현재 단국대학교 신소재공학과 석사과정 재학

⊙⊙ 정 서 인
⊙ 2022년 단국대학교 신소재공학과 학사
⊙ 현재 단국대학교 신소재공학과 석사과정 재학

⊙⊙ 김 희 진
⊙ 현재 단국대학교 신소재공학과 학사과정 재학

⊙⊙ 박 희 정
⊙ 2000년 한양공대 신소재공학과 학사
⊙ 2005년 포항공대 신소재공학과 박사
⊙ 2015년 삼성전자종합기술원 전문연구원
⊙ 현재 단국대학교 신소재공학과 교수